Co je anoda a katoda - jednoduché vysvětlení
Elektrochemie a galvanizace
V elektrochemii existují dvě hlavní sekce:
- Galvanické články - výroba elektřiny chemickou reakcí. Tyto prvky zahrnují baterie a akumulátory. Často se nazývají chemické zdroje proudu.
- Elektrolýza - zkráceně dopad na chemickou reakci s elektřinou - pomocí zdroje energie začíná reakce.
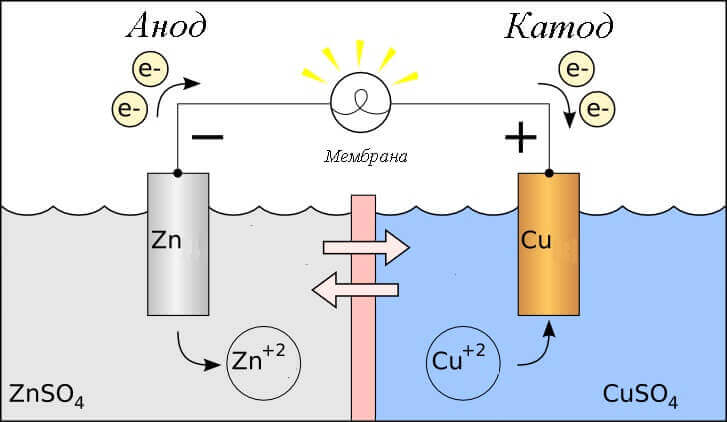
Zvažte redoxní reakci v galvanickém článku, jaké procesy se tedy vyskytují na jeho elektrodách?
- Anoda - elektroda, na které je pozorována oxidační reakceto je ondává elektrony. Elektroda, na které oxidační reakce probíhá, se nazývá redukční činidlo.
- Cathode - elektroda, na které teče regenerační reakceto je onpřijímá elektrony. Elektroda, na které nastává redukční reakce, se nazývá oxidační činidlo.
To vyvolává otázku - kde je plus a kde je minus baterie? Na základě definice galvanického článku anoda dává elektrony.
Důležité! GOST 15596-82 uvádí oficiální definici názvů závěrů chemických zdrojů proudu, zkrátka pak plus na katodě a minus na anodě.
V tomto případě se uvažuje tok elektrického proudu. podél vodiče vnějšího obvodu z oxidační činidlo (katoda) do redukční činidlo (anoda). Protože elektrony v obvodu tečou z mínus na plus a elektrický proud je obráceně, pak je katoda plus a anoda je mínus.
Pozor: proud vždy teče do anody!
Nebo to samé v diagramu:
Elektrolýza baterií nebo proces nabíjení
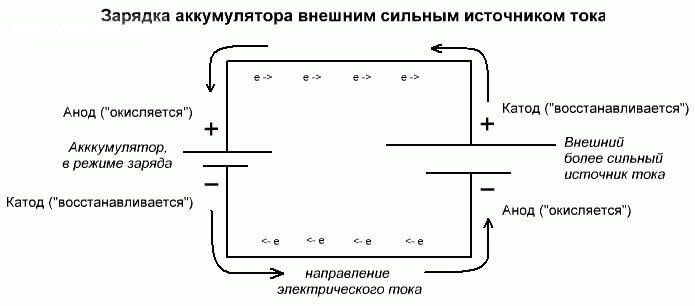
Tyto procesy jsou podobné a inverzní k galvanickému článku, protože zde ne energie pochází z chemické reakce, ale spíše k chemické reakci dochází z vnějšího zdroje elektřiny.
V tomto případě se navíc zdroj energie nazývá také katoda a mínus anoda. Ale kontakty nabíjecího galvanického článku nebo elektrod elektrolyzéru již budou mít opačná jména, uvidíme proč!
Důležité! Při vybití galvanického článku je anoda mínus, katoda je plus a obráceně při nabíjení.
Protože proud z kladného pólu zdroje energie je přiváděn do kladného pólu baterie, nemůže být tato baterie katodou.Z výše uvedeného vyplývá, že v tomto případě se elektrody baterie při nabíjení podmíněně mění.
Potom se elektrodou nabitého galvanického článku, do kterého proudí elektrický proud, nazývá anoda. Ukázalo se, že při nabíjení baterie se plus stává anodou a mínus katodou.
Galvanizace
Procesy depozice kovů v důsledku chemické reakce pod vlivem elektrického proudu (během elektrolýzy) se nazývají galvanické inženýrství. Svět tak získal stříbrné, pozlacené, chromované nebo jiné kovové pokovené šperky a detaily. Tento proces se používá jak pro dekorativní, tak i pro aplikované účely - ke zlepšení odolnosti různých komponent a sestav mechanismů proti korozi.
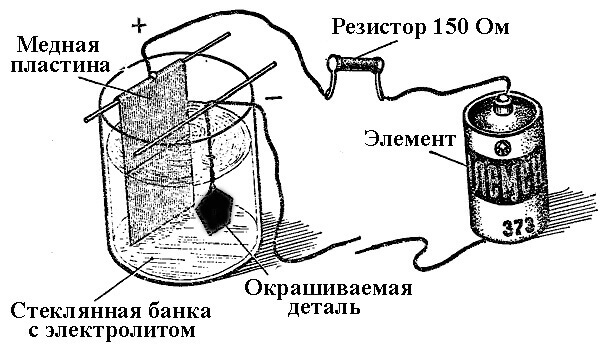
Princip činnosti elektrolytických zařízení spočívá v použití solných roztoků prvků, které zakrývají součást jako elektrolyt.
Při elektrolytickém pokovování je anodou také elektroda, ke které je připojen kladný výstup zdroje energie, v tomto případě je katoda mínus. V tomto případě je kov ukládán (redukován) na zápornou elektrodu (redukční reakce). To znamená, že pokud si přejete vyrobit zlacený prsten vlastními rukama - připojte k němu záporný výstup napájení a umístěte jej do nádoby s vhodným řešením.
V elektronice
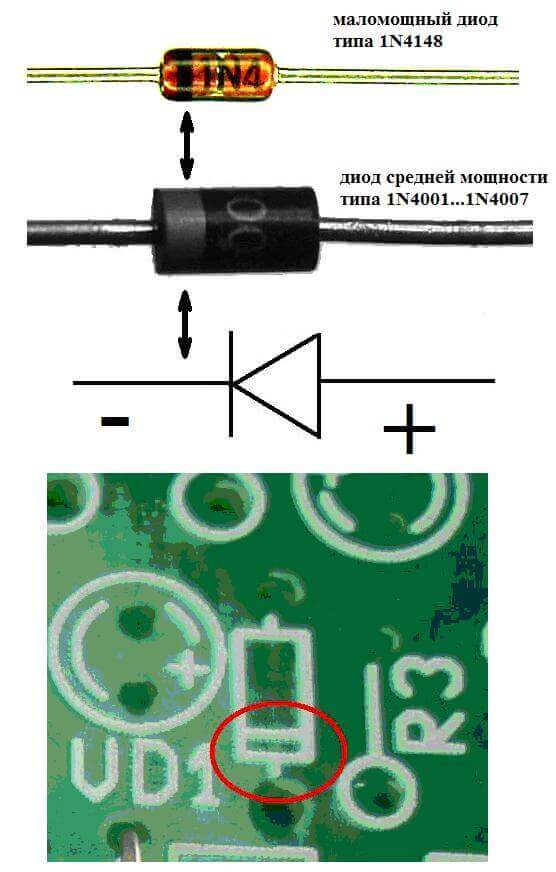
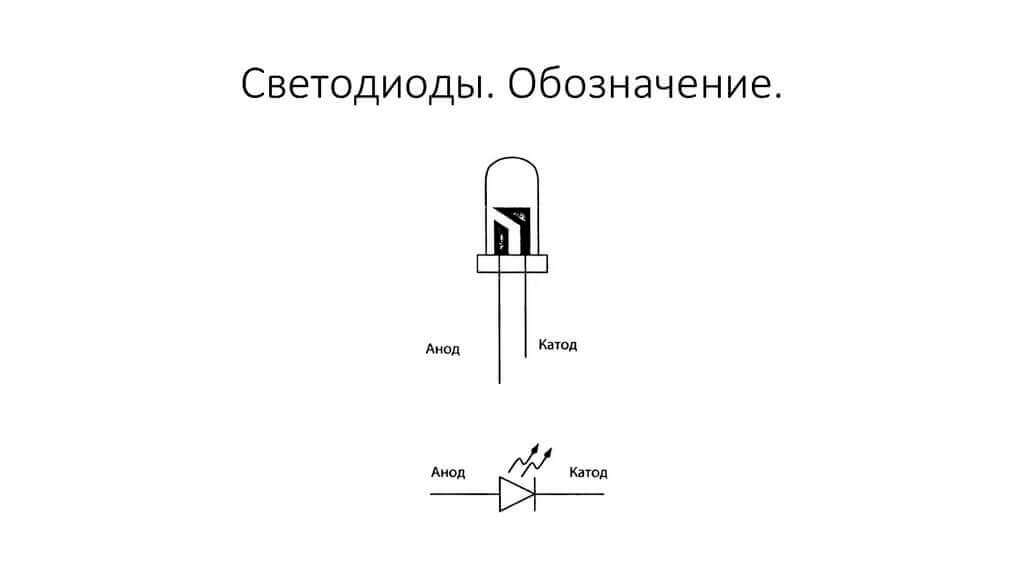
Elektrody nebo nohy polovodičových a vakuových elektronických zařízení se také často nazývají anoda a katoda. Zvažte podmíněné grafické označení polovodičové diody v diagramu:
Jak vidíme, anoda diody je připojena k plusu baterie. To se nazývá ze stejného důvodu - v tomto případě proud v každém případě proudí na výstup diody. Na skutečném prvku na katodě je označení ve formě proužku nebo tečky.
LED je podobná. Na 5 mm LED diodách jsou vnitřky viditelné skrz baňku. Polovina, která je větší, je katoda.
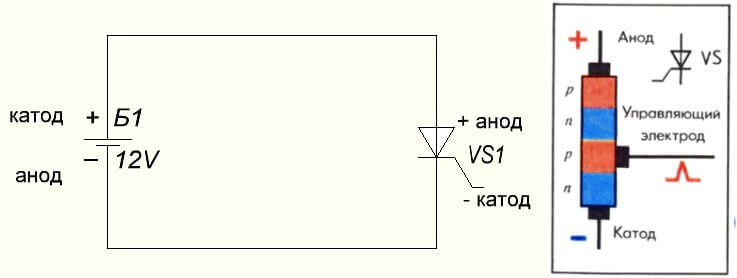
Situace je také s tyristorem, účelem závěrů a „unipolární“ aplikací těchto třínohých komponentů z něj činí řízenou diodu:
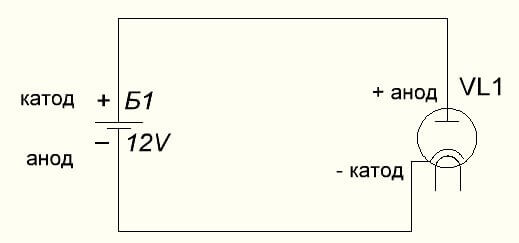
Vakuová dioda také spojuje anodu s plusem a katodu s mínusem, což je znázorněno na obrázku níže. Přestože při použití zpětného napětí se názvy těchto prvků nezmění, navzdory proudu elektrického proudu v opačném směru, byť nevýznamné.
U pasivních prvků, jako jsou kondenzátory a rezistory, tomu tak není. Katoda a anoda nejsou izolovány odděleně od rezistoru, proud v ní může proudit v libovolném směru. Její závěry můžete pojmenovat podle situace a systému. Také běžné nepolární kondenzátory. Méně často je toto oddělení kontaktních jmen pozorováno u elektrolytických kondenzátorů.
Závěr
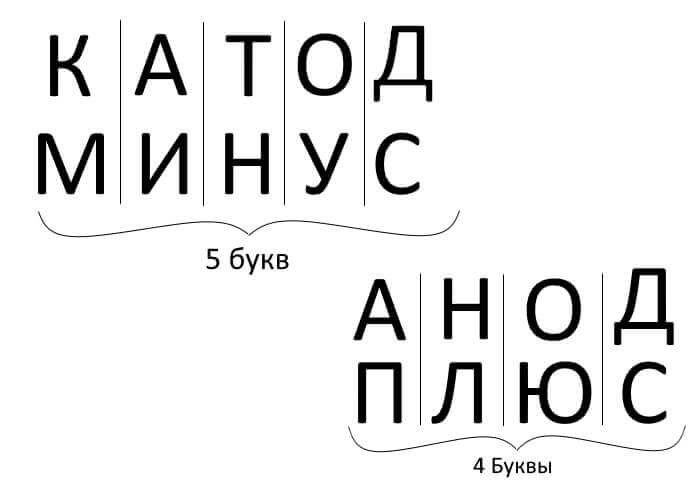
Abychom to shrnuli, odpovíme na otázku: jak si vzpomenout, kde je plus, kde je minus katody s anodou? Existuje vhodné mnemonické pravidlo pro elektrolýzu, nabíjení baterie, galvanické a polovodičové zařízení. Tato slova s podobnými jmény mají stejný počet písmen, jak je znázorněno níže:
Ve všech těchto případech proud teče z katody a teče do anody.
Nenechte se zmást zmatkem: „Proč je katoda pozitivní pro baterii a když je nabitá, stane se negativní?“ Nezapomeňte na všechny prvky elektroniky, elektrolyzéry a na galvanické pokovování - obecně pro všechny spotřebitele energie je anoda výstupem připojeným k plusu. Rozdíly zde končí, nyní je pro vás snazší zjistit, jaké jsou klady a zápory mezi výstupy prvků a zařízení.
Nakonec doporučujeme sledovat užitečné video k tématu článku:
Nyní víte, co jsou anody a katody, a jak si je pamatovat dostatečně rychle. Doufáme, že poskytnuté informace byly pro vás užitečné a zajímavé!
Související materiály: