¿Qué es el ánodo y el cátodo? Una explicación simple
Electroquímica y galvanoplastia
Hay dos secciones principales en electroquímica:
- Células galvánicas: la producción de electricidad a través de una reacción química. Estos elementos incluyen baterías y acumuladores. A menudo se les llama fuentes químicas de corriente.
- Electrólisis: el impacto en una reacción química con electricidad, en palabras simples, con la ayuda de una fuente de energía, se inicia una reacción.
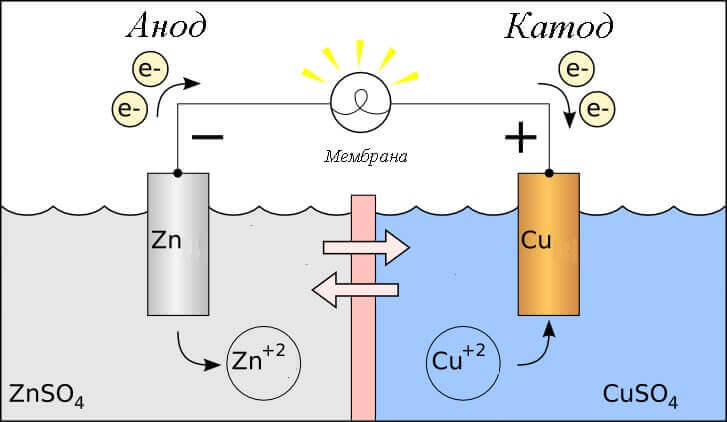
Considere la reacción redox en una celda galvánica, entonces, ¿qué procesos ocurren en sus electrodos?
- Ánodo - el electrodo en el que se observa reacción oxidativaes decir, élda electrones. El electrodo en el que se produce la reacción de oxidación se llama agente reductor.
- Cátodo - el electrodo sobre el que fluye reacción de recuperaciónes decir, élacepta electrones. El electrodo en el que se produce la reacción de reducción se llama agente oxidante.
Esto plantea la pregunta: ¿dónde está el plus y dónde está el menos de la batería? Basado en la definición de una celda galvánica ánodo da electrones.
Importante! GOST 15596-82 ofrece una definición oficial de los nombres de las conclusiones de las fuentes de corriente química, en resumen, más en el cátodo y menos en el ánodo.
En este caso, se considera el flujo de corriente eléctrica. a lo largo del conductor del circuito externo de oxidante (cátodo) a reductor (ánodo). Dado que los electrones en el circuito fluyen de menos a más, y la corriente eléctrica es viceversa, entonces el cátodo es un más, y el ánodo es un menos.
Atención: ¡La corriente siempre fluye hacia el ánodo!
O lo mismo en el diagrama:
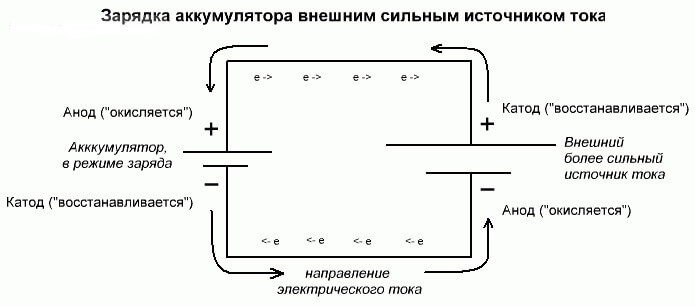
Electrólisis de batería o proceso de carga.
Estos procesos son similares e inversos a la célula galvánica, ya que aquí la energía no proviene de una reacción química, sino que se produce una reacción química debido a una fuente externa de electricidad.
En este caso, más la fuente de alimentación también se llama cátodo, y menos el ánodo. Pero los contactos de la celda galvánica recargable o los electrodos del electrolizador ya tendrán nombres opuestos, ¡veamos por qué!
Importante! Cuando se descarga una celda galvánica, el ánodo es negativo, el cátodo es positivo y viceversa al cargar.
Dado que la corriente del terminal positivo de la fuente de alimentación se suministra al terminal positivo de la batería, esta última ya no puede ser un cátodo.Refiriéndonos a lo anterior, podemos concluir que en este caso los electrodos de la batería cambian de lugar condicionalmente durante la carga.
Luego, a través del electrodo de una celda galvánica cargada dentro de la cual fluye una corriente eléctrica, se llama ánodo. Resulta que al cargar la batería, el más se convierte en el ánodo y el menos el cátodo.
Galvanoplastia
Los procesos de deposición de metales como resultado de una reacción química bajo la influencia de una corriente eléctrica (durante la electrólisis) se denominan ingeniería galvánica. Por lo tanto, el mundo recibió joyas y detalles plateados, dorados, cromados u otros chapados en metal. Este proceso se utiliza tanto para fines decorativos como aplicados, para mejorar la resistencia a la corrosión de varios componentes y conjuntos de mecanismos.
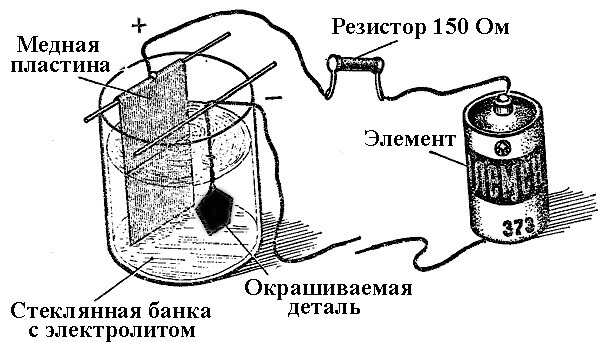
El principio de funcionamiento de las plantas de galvanoplastia reside en el uso de soluciones salinas de los elementos que cubrirán la pieza como electrolito.
En galvanoplastia, el ánodo es también un electrodo al que está conectada la salida positiva de la fuente de alimentación, respectivamente, el cátodo en este caso es un signo negativo. En este caso, el metal se deposita (reduce) en el electrodo negativo (reacción de reducción). Es decir, si desea hacer un anillo dorado con sus propias manos, conecte la salida negativa de la fuente de alimentación y colóquelo en un recipiente con la solución adecuada.
En electronica
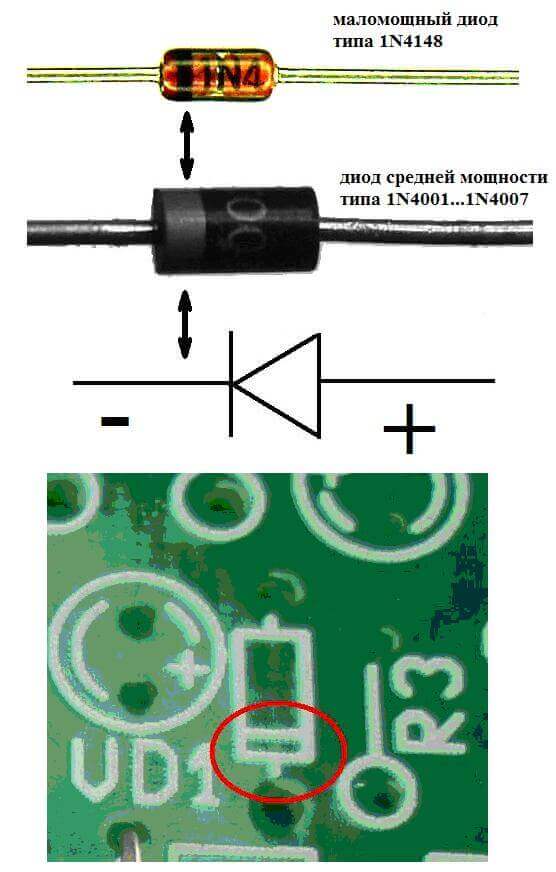
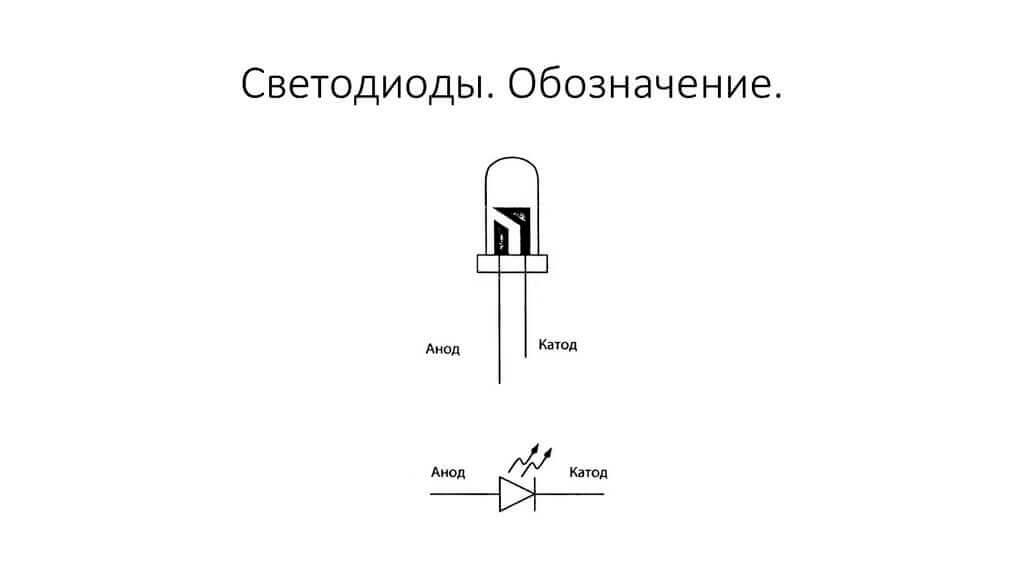
Los electrodos o patas de los dispositivos electrónicos de semiconductores y vacío también suelen denominarse ánodo y cátodo. Considere la designación gráfica condicional de un diodo semiconductor en el diagrama:
Como vemos, el ánodo del diodo está conectado al plus de la batería. Se llama así por la misma razón: en este caso, la corriente fluye hacia la salida del diodo en cualquier caso. En un elemento real del cátodo hay una marca en forma de tira o punto.
El LED es similar. En los LED de 5 mm, el interior es visible a través del matraz. La mitad que es más grande es el cátodo.
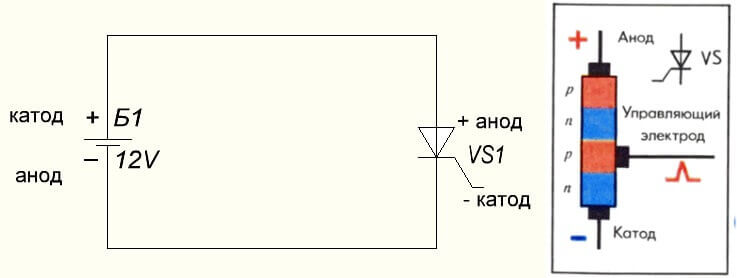
La situación también es con el tiristor, el propósito de las conclusiones y la aplicación "unipolar" de estos componentes de tres patas lo convierten en un diodo controlado:
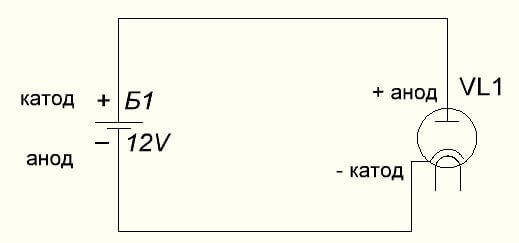
El diodo de vacío también conecta el ánodo al más, y el cátodo al menos, que se muestra en el siguiente diagrama. Aunque al aplicar voltaje inverso, los nombres de estos elementos no cambiarán, a pesar del flujo de corriente eléctrica en la dirección opuesta, aunque sea insignificante.
Con elementos pasivos como condensadores y resistencias, este no es el caso. El cátodo y el ánodo no están aislados por separado de la resistencia; la corriente puede fluir en cualquier dirección. Puede dar cualquier nombre a sus conclusiones, según la situación y el esquema en cuestión. Condensadores no polares convencionales también. Con menos frecuencia, esta separación de nombres de contacto se observa en condensadores electrolíticos.
Conclusión
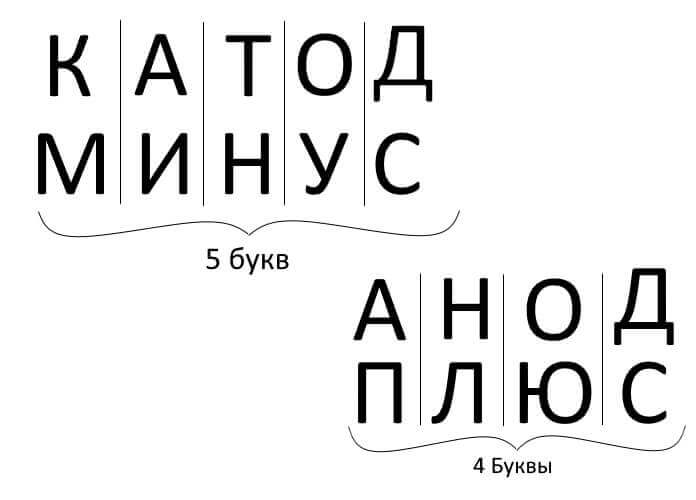
Entonces, para resumir, respondiendo la pregunta: ¿cómo recordar dónde está el más, dónde está el menos del cátodo con el ánodo? Existe una regla mnemónica conveniente para electrólisis, carga de batería, galvanoplastia y dispositivos semiconductores. Estas palabras con nombres similares tienen el mismo número de letras, como se ilustra a continuación:
En todos estos casos, la corriente fluye desde el cátodo y fluye hacia el ánodo.
No se confunda con la confusión: "¿por qué el cátodo es positivo para la batería, y cuando se carga, se vuelve negativo?" Recuerde para todos los elementos de la electrónica, así como los electrolizadores y en galvanoplastia; en general, para todos los consumidores de energía, el ánodo es la salida conectada al plus. Las diferencias terminan allí, ahora es más fácil para usted descubrir cuál es el más y el menos entre las salidas de los elementos y dispositivos.
Finalmente, recomendamos ver un video útil sobre el tema del artículo:
Ahora ya sabe qué son el ánodo y el cátodo, así como también cómo recordarlos lo suficientemente rápido. ¡Esperamos que la información proporcionada sea útil e interesante para usted!
Materiales relacionados: